Idrocarburi
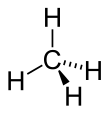
La struttura di una molecola di metano, il più semplice idrocarburo della classe degli alcani.
Gli idrocarburi sono composti organici che contengono soltanto atomi di carbonio e di idrogeno.[1][2]
Ampiamente usati come combustibili, la loro principale fonte in natura è di origine fossile.
Indice
1 Caratteristiche
2 Classificazione degli idrocarburi
2.1 Idrocarburi alifatici
2.2 Idrocarburi aromatici
3 Proprietà
3.1 Stato di aggregazione
3.2 Stabilità/reattività
3.3 Polarità
4 Separazione degli idrocarburi
5 Processi chimici che coinvolgono gli idrocarburi
6 Aspetti economici e geopolitici
7 Note
8 Bibliografia
9 Voci correlate
10 Altri progetti
11 Collegamenti esterni
Caratteristiche |
Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di idrogeno (H) sporgono da questo scheletro. Gli idrocarburi sono l'unica categoria di composti organici privi del gruppo funzionale, sono infatti composti solamente da atomi di idrogeno e carbonio.
All'aumentare del numero di atomi di carbonio presenti nella catena idrocarburica aumenta il numero di composti idrocarburici possibili.
La catena più corta possibile è composta da un solo atomo di carbonio, a cui corrisponde il metano, avente formula bruta CH4.
Gli idrocarburi aventi due atomi di carbonio sono tre:
- l'etano, di formula C2H6
- l'etene (o etilene), C2H4
- l'etino (o acetilene), C2H2.
Questi tre idrocarburi si differenziano per il numero di legami che tengono uniti i due atomi di carbonio contigui: un legame (per cui si parla di "legame semplice") nel caso dell'etano, due legami ("legame doppio") nel caso dell'etilene e tre legami ("legame triplo") nel caso dell'acetilene.
Nella struttura di un generico idrocarburo ogni atomo di carbonio usa da uno a tre elettroni di valenza per formare legami con il carbonio adiacente, mentre i restanti elettroni di valenza del carbonio sono utilizzati per formare i legami con gli atomi di idrogeno. All'interno della molecola idrocarburica possono esserci comunque degli atomi di carbonio a cui non sono legati atomi di idrogeno, ma solo altri atomi di carbonio (un esempio è l'atomo di carbonio centrale della molecola di neopentano).
Classificazione degli idrocarburi |
Una prima distinzione tra i vari idrocarburi si riferisce al loro stato fisico nelle condizioni di pressione e di temperatura ambientali e cioè:
- Idrocarburi solidi o semisolidi: costituenti dell'asfalto, del bitume, cere paraffiniche, ecc.
- Idrocarburi liquidi: costituenti del petrolio (grezzo), benzene, esano, ottano, ecc.
- Idrocarburi gassosi: metano, etano, propano, butano, ecc.
Dal punto di vista delle proprietà chimiche, gli idrocarburi si distinguono in due classi principali:
- idrocarburi aromatici: dotati di "aromaticità", una proprietà chimica impartita da un anello benzenico, che li rende particolarmente stabili;[1]
- idrocarburi alifatici: non dotati di aromaticità.
Le varie tipologie di idrocarburi (alcani, alcheni, ecc.) descritte di seguito vengono dette "serie omologhe".
La classificazione qui descritta non vuole essere esaustiva, infatti esistono tante tipologie di idrocarburi non bene classificabili, quali ad esempio i catenani, che sono costituiti da più anelli inseriti l'uno nell'altro in modo che ognuno possa muoversi indipendentemente dall'altro ma senza "sciogliersi" (in maniera analoga agli anelli di una catena in acciaio, da cui il nome).[3]
Idrocarburi alifatici |
.mw-parser-output .vedi-anche{border:1px solid #CCC;font-size:95%;margin-bottom:.5em}.mw-parser-output .vedi-anche td:first-child{padding:0 .5em}.mw-parser-output .vedi-anche td:last-child{width:100%}
A seconda dei tipi di legame C-C presenti nella molecola (singolo, doppio o triplo) e della loro geometria (lineare, ramificata, ciclica), gli idrocarburi alifatici si dividono inoltre in:[1]
idrocarburi saturi: con soli legami singoli C-C[4]
alcani (o paraffine): idrocarburi saturi non ciclici, cioè aventi una catena non richiusa su sé stessa; hanno formula generale CnH2n+2. A loro volta possono essere lineari o ramificati, a seconda che gli atomi di carbonio si susseguano in maniera continua o con biforcazioni
cicloalcani: idrocarburi saturi ciclici, aventi formula generale CnH2n[5]
bicicloalcani: idrocarburi saturi costituiti da due catene cicliche contigue[5]
alchilcicloalcani: idrocarburi saturi costituiti da una catena idrocarburica ciclica legata ad una catena non ciclica)[6]

Formula di struttura del butano (un alcano)
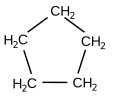
Formula di struttura del ciclopentano (un cicloalcano)
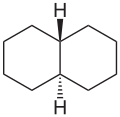
Formula di struttura della decalina (un bicicloalcano)
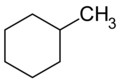
Formula di struttura del metilcicloesano (un alchilcicloalcano)
idrocarburi insaturi: contengono almeno un legame C-C multiplo (cioè doppio o triplo)[4]. I legami formati da due o più atomi presenti nella catena del carbonio che costituisce lo scheletro della molecola hanno geometria trigonale perché sono ibridati sp2, oppure hanno geometria lineare perché sono ibridati sp; nello scheletro della molecola è presente almeno un doppio legame, σ + π;
alcheni (o olefine): non ciclici e con un legame doppio C=C, aventi formula generale CnH2n
dieni (o alcadieni), trieni (o alcatrieni), polieni: non ciclici e aventi rispettivamente due, tre o molti legami doppi C=C
cicloalcheni: ciclici, con un legame doppio C=C, aventi formula generale CnH2n-2
alchini: non ciclici e con un legame triplo C≡C, aventi formula generale CnH2n-2
cicloalchini: ciclici, con un legame triplo, aventi formula generale CnH2n-4.
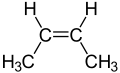
Formula di struttura del butene (un alchene)
Formula di struttura del butadiene (un diene)
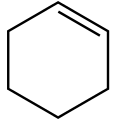
Formula di struttura del cicloesene (un cicloalchene)

Formula di struttura dell'acetilene (un alchino)
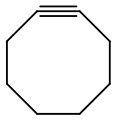
Formula di struttura del cicloottino (un cicloalchino)
Gli idrocarburi alifatici ciclici sono detti idrocarburi aliciclici.
Idrocarburi aromatici |
A seconda del tipo di struttura, gli idrocarburi aromatici si possono dividere in:
benzene e derivati
idrocarburi aromatici polinucleati (o "policiclici")

Formula di struttura del benzene (un idrocarburo aromatico)

Formula di struttura del cumene (un derivato del benzene)
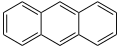
Formula di struttura dell'antracene (un idrocarburo aromatico polinucleato)
Proprietà |
In generale per gli alcani aciclici, quelli con peso molecolare simile hanno proprietà chimico-fisiche simili.
Esistono in natura varie miscele di idrocarburi, con caratteristhe chimico-fisiche intermedie fra una categoria e l'altra.
Stato di aggregazione |
Lo stato di aggregazione degli idrocarburi (a temperatura e pressione ambiente) dipende dal loro peso molecolare: gli idrocarburi aventi peso molecolare minore (ad esempio metano, etano, propano) si trovano allo stato gassoso, quelli con peso molecolare più elevato (ad esempio benzene, esano e ottano) sono liquidi e quelli aventi peso molecolare ancora più elevato sono solidi cerosi.

Bombole contenenti GPL, una miscela di idrocarburi normalmente gassosi mantenuti allo stato liquido dalle elevate pressioni in cui si trovano.
Spesso gli idrocarburi che a temperatura e pressione sono sotto forma di gas vengono mantenuti all'interno di recipienti in pressione (ad esempio in bombole), in modo da conservarli in volumi più ristretti. Infatti, a parità di temperatura e quantità di sostanza, all'aumentare della pressione diminuisce il volume occupato da un gas (come deducibile dall'equazione di stato dei gas perfetti o da altre equazioni di stato), finché esso passa (in parte o in toto) allo stato liquido. Ad esempio le comuni "bombole del gas" utilizzate in ambito domestico contengono una miscela liquida di idrocarburi (nota come GPL) che si trovano gassosi a temperatura e pressione ambiente.
Stabilità/reattività |
Gli idrocarburi ciclici formati da meno di sei atomi di carbonio sono particolarmente instabili a causa della piccolezza dell'anello, che si traduce in una elevata tensione d'anello (o "tensione angolare"), ovvero un'elevata energia immagazzinata nella molecola che tende ad aprire l'anello.[7]
In generale gli idrocarburi saturi, benché siano facilmente infiammabili e quindi reagiscano facilmente con l'ossigeno, hanno una relativa inerzia chimica; per tale motivo sono stati denominati originariamente paraffine (dal latino parum affinis, "poco reattivo").[8]
Gli idrocarburi contenenti insaturazioni hanno altre proprietà, dovute ai doppi o tripli legami e sono chimicamente più reattivi nelle posizioni contenenti il doppio o triplo legame o immediatamente adiacenti ad esse.
Gli idrocarburi aromatici formano una classe a sé per stabilità ed hanno una reattività chimica molto diversa da quella degli idrocarburi alifatici.
Polarità |
Le molecole degli alcani e dei cicloalcani sono apolari, in quanto, anche se il legame covalente C-H è polarizzato, la differenza di elettronegatività è piuttosto bassa (0,4) e la struttura tetraedrica porta a una distribuzione della carica nelle molecole complessivamente simmetrica.
Le considerazioni sulla loro struttura molecolare trovano conferma nelle prove di solubilità: gli alcani sono praticamente insolubili in acqua, mentre si sciolgono nei solventi apolari.
Separazione degli idrocarburi |

Schema semplificato del processo di distillazione del greggio
Moltissimi idrocarburi derivano dal processo di raffinazione del petrolio, che consiste in un insieme di processi chimico-fisici che hanno lo scopo di ottenere determinati prodotti chimici (miscele combustibili, asfalto, lubrificanti, ecc.) a partire dal greggio.
Tra i vari processi impiegati nella raffinazione, la distillazione del greggio (o "topping") riveste un ruolo fondamentale. Nella colonna di distillazione il greggio viene separato in più "tagli", a seconda del peso molecolare (o a volere essere più precisi, della volatilità) degli idrocarburi che costituiscono il taglio in questione. Ogni taglio viene individuato dal numero di atomi di carbonio che sono contenuti nelle molecole del taglio in questione. Ad esempio il taglio C4 contiene idrocarburi che hanno quattro atomi di carbonio (come ad esempio il butano, il butene e i loro isomeri). Questo perché è molto più difficile separare per mezzo della sola distillazione molecole idrocarburiche che abbiano pesi molecolari vicini o addirittura identici. Ciò riflette il fatto che idrocarburi simili (cioè appartenenti alla stessa serie omologa) hanno proprietà chimico-fisiche simili tra loro.
Processi chimici che coinvolgono gli idrocarburi |
Gli idrocarburi sono una classe talmente ampia di composti che è impossibile citare tutte le reazioni in campo industriale nelle quali possono essere coinvolti.
Tra le moltissime reazioni che coinvolgono gli idrocarburi, si annoverano le seguenti:
cracking: è un processo chimico industriale rivolto alla formazione di paraffine a basso peso molecolare a partire da paraffine ad elevato peso molecolare;
reforming catalitico: è un processo che mira ad ottenere un prodotto avente un numero di ottano più elevato. A partire da paraffine si ha formazione di olefine, aromatici, isomeri ramificati e molecole a catena più corta;
polimerizzazione: si sfrutta per l'ottenimento di polimeri, ovvero molecole aventi pesi molecolari elevatissimi; polimeri di natura idrocarburica sono ad esempio il polietilene e il polipropilene.
Aspetti economici e geopolitici |
Tutti gli idrocarburi assumono un'enorme importanza nell'economia e nella geopolitica moderne, principalmente grazie al loro ruolo fondamentale come fonte d'energia e per le vastissime applicazioni di tipo industriale.
Note |
^ abc Solomons, p. 42
^ (EN) IUPAC Gold Book, "hydrocarbons"
^ Solomons, p. 106
^ ab Callister, pp. 445-446
^ ab Solomons, p. 93
^ Solomons, p. 94
^ Solomons, p. 102
^ Solomons, p. 123
Bibliografia |
- T. W. Graham Solomons, Chimica organica, a cura di G. Ortaggi, D. Misiti, 2ª ed., Bologna, Zanichelli, 1988, ISBN 88-08-09414-6.
- (EN) William D. Callister, Material Science and Engineering: An Introduction, 5ª ed., John Wiley & Sons Inc, 1999, ISBN 0-471-35243-8.
Voci correlate |
- Petrolio
- Combustibili fossili
- Gas naturale
- Composti organici
- Origine abiotica del petrolio
- Stufa a idrocarburi
- Polimero
Altri progetti |
Altri progetti
- Wikizionario
- Wikimedia Commons
 Wikizionario contiene il lemma di dizionario «idrocarburi»
Wikizionario contiene il lemma di dizionario «idrocarburi»
 Wikimedia Commons contiene immagini o altri file su idrocarburi
Wikimedia Commons contiene immagini o altri file su idrocarburi
Collegamenti esterni |
Idrocarburi, su thes.bncf.firenze.sbn.it, Biblioteca Nazionale Centrale di Firenze.
(EN) Idrocarburi, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Tipologia e struttura degli idrocarburi (PDF), su treccani.it.
- MSN Encarta - Idrocarburi, su it.encarta.msn.com.
- Sapere.it - Idrocarburi, su sapere.it.
- (EN) Molecular Structures of Organic Compounds - Hydrocarbons, su csi.chemie.tu-darmstadt.de.
.mw-parser-output .navbox{border:1px solid #aaa;clear:both;margin:auto;padding:2px;width:100%}.mw-parser-output .navbox th{padding-left:1em;padding-right:1em;text-align:center}.mw-parser-output .navbox>tbody>tr:first-child>th{background:#ccf;font-size:90%;width:100%}.mw-parser-output .navbox_navbar{float:left;margin:0;padding:0 10px 0 0;text-align:left;width:6em}.mw-parser-output .navbox_title{font-size:110%}.mw-parser-output .navbox_abovebelow{background:#ddf;font-size:90%;font-weight:normal}.mw-parser-output .navbox_group{background:#ddf;font-size:90%;padding:0 10px;white-space:nowrap}.mw-parser-output .navbox_list{font-size:90%;width:100%}.mw-parser-output .navbox_odd{background:#fdfdfd}.mw-parser-output .navbox_even{background:#f7f7f7}.mw-parser-output .navbox_center{text-align:center}.mw-parser-output .navbox .navbox_image{padding-left:7px;vertical-align:middle;width:0}.mw-parser-output .navbox+.navbox{margin-top:-1px}.mw-parser-output .navbox .mw-collapsible-toggle{font-weight:normal;text-align:right;width:7em}.mw-parser-output .subnavbox{margin:-3px;width:100%}.mw-parser-output .subnavbox_group{background:#ddf;padding:0 10px}
.mw-parser-output .CdA{border:1px solid #aaa;width:100%;margin:auto;font-size:90%;padding:2px}.mw-parser-output .CdA th{background-color:#ddddff;font-weight:bold;width:20%}
| Controllo di autorità | LCCN (EN) sh85063372 · GND (DE) 4125165-9 |
|---|









